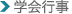| 卵白リゾチームの場合、育成温度を 7 °C と低くするとバルク結晶(正方晶リゾチーム)と共にスフェルライト状の結晶が晶出する(Fig.1a)。 Fig.1a に見られるように、二つの晶出相は異なる形態を有しており、結晶構造が異なっている可能性が高い。 タンパク質結晶内には多量の水分子が存在し、結晶構造の違いによりその量が異なることが知られている。 例えば、卵白リゾチームの場合、正方晶系では結晶内には 39 vol.% の水分子が存在するが、斜方晶系では 43 vol.% 存在する。 このようなタンパク質結晶内の水分子の含有量の違いは、結晶の誘電緩和にも影響を与え、 水分子の含有量が増加すると誘電緩和を起こす周波数が、高周波数側にシフトすることが示唆されている。 加えて、誘電緩和の起きる原因が結晶内の水素結合ネットワークに起因しているのならば、水分子の含有量が多い結晶では、 その分大きな誘電損失を生じるはずである。 ゆえに、水分子の含有量が多い結晶の方が、高周波数側で誘電率が低くなる可能性があり、 結晶多形間では、Fig.1b に示されるような誘電率の周波数依存性の関係が期待できる。 つまり、二つの固相間の誘電率の大小関係を印加周波数によって操作することにより、晶出相の制御が可能なのである。 |
|
| Fig.1 (a) Optical micrograph of bulk and spherulitic crystals of HEWL coexisting in a droplet of solution. (b) Schematic diagram of the predicted dependence of the permittivity of the two different solid phases on the frequency of the applied electric field. |
|
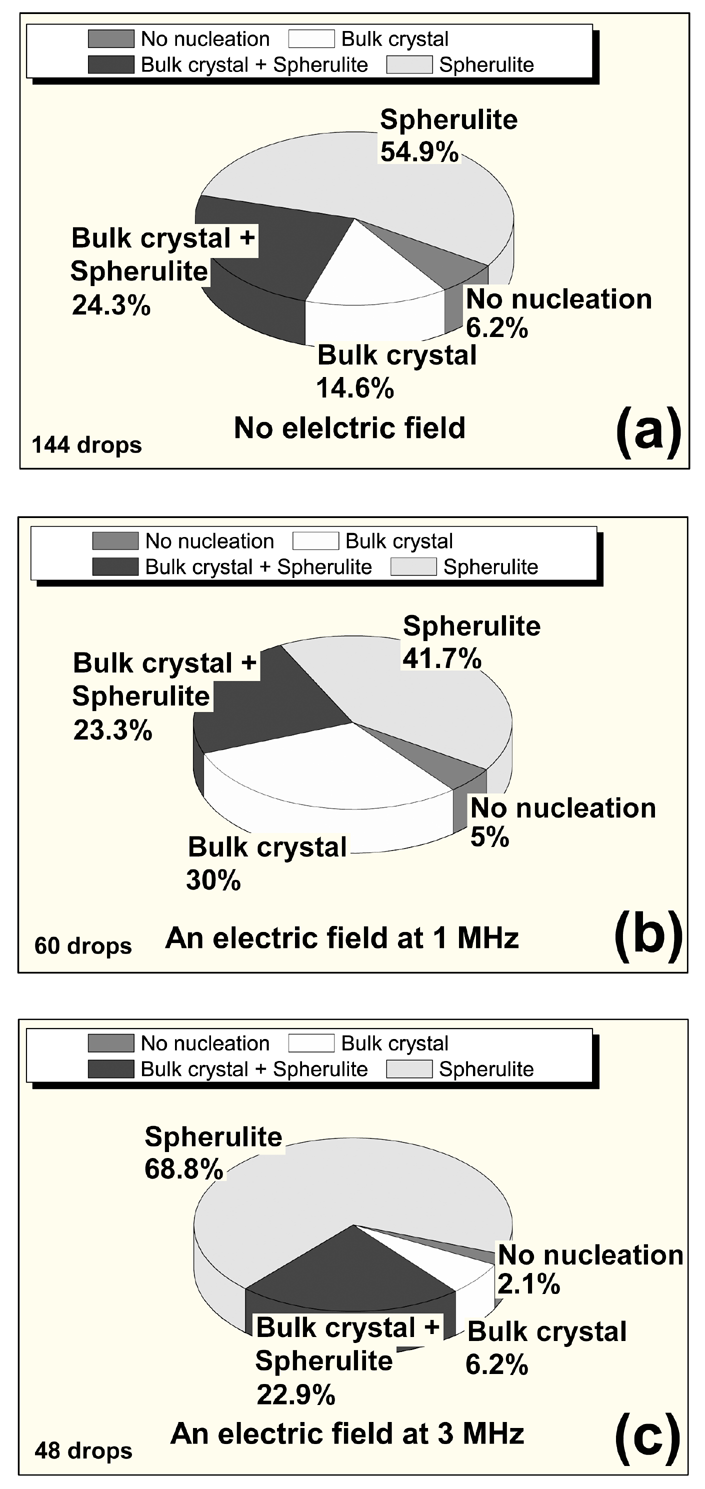
Fig.2 に電場印加ありと電場印加なしのときのドロップ中に形成される 4 種類の晶出相の分布を示す。
また、Fig.2 の各々の図の左下に観察されたドロップ数を示す。はじめに、電場印加なしのときの晶出相の分布に焦点を当てる。
Fig.2a に示されているように、スフェルライトの晶出割合は、バルク結晶のものよりも大きいことが分かる。
この結果は、以下の二つのどちらかの可能性に起因しており、
それは (a) スフェルライトの化学ポテンシャルがバルク結晶のものよりも非常に小さく、
このため、スフェルライトにおける核形成のための駆動力、 Fig.2b に見られるように、1 MHz 印加時において、タンパク質ドロップ内に形成されたバルク結晶の晶出割合は、 電場印加なしに比べより大きく、これに対し、スフェルライトの晶出割合は減少していた。 これは、バルク結晶における核形成のための駆動力が、1 MHz の交流電場印加時において、 スフェルライトのものよりも大きくなったことを示唆している。 これに対し、Fig.2c に見られるように、3 MHz 印加時においては、スフェルライトの晶出割合は電場印加なしのときと比べ増加し、 バルク結晶の晶出割合は逆の傾向を示した。 これは、3 MHz の交流電場を印加することによって、スフェルライトに比べて、バルク結晶では核形成のための駆動力が小さくなったことを反映している。 最後に、交流電場印加によってタンパク質ドロップ中に形成された晶出相の分布がどのように変化したのかを考察する。 これまでと同様に、三相間の誘電率の大小関係が、交流電場を印加したときの液相と二つの固相の G 曲線の変化の度合いを決定しており、 これに対し、誘電率の組成依存性の符号が、三相すべての G 曲線のシフトの方向を決定している。 つまり、液相と固相の誘電率の組成依存性の符号は、どちらも負であるため、 交流電場印加によって G 曲線が最も下にシフトした相が、最も晶出し易い相となる。 |
|
| Fig.2 The distribution of the phases formed in solution droplets, with and without application of an external electric field. (a) No electric field, and applied fields at (b) 1 MHz, and (c) 3 MHz. |
|
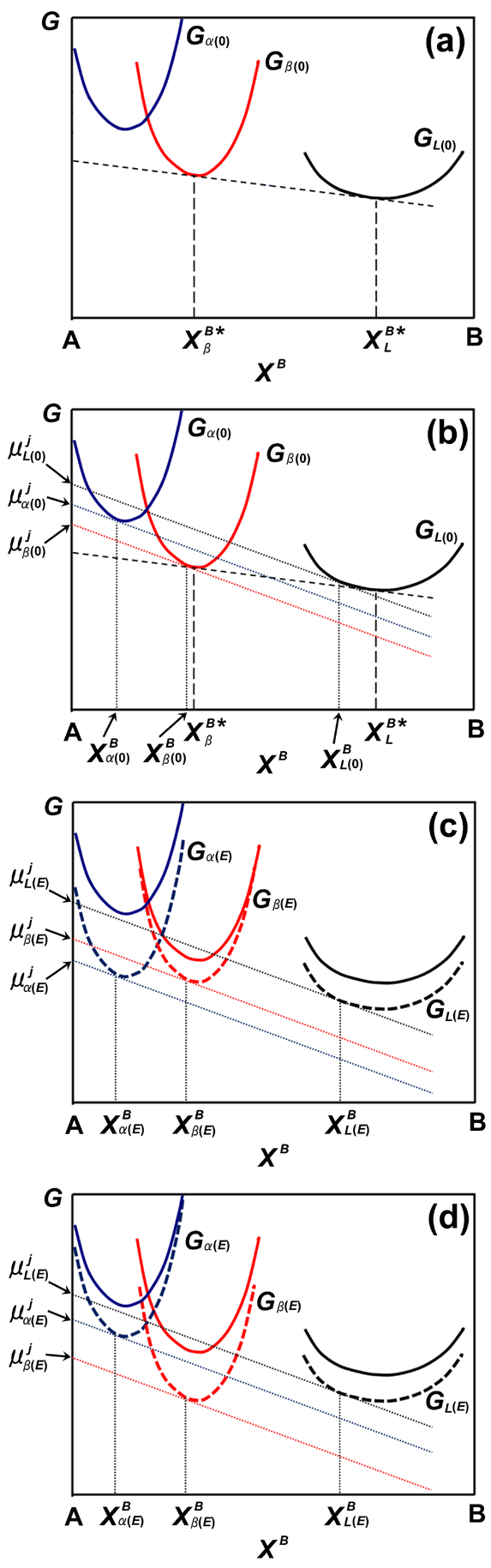
ここで、Fig.3 に示されているような二成分系での液相、α 相および β 相のモル自由エネルギーについて考える。
Fig.3 内の組成 A と組成 B はそれぞれタンパク質と水を表している。
また、 G 曲線を表している。 Fig.3a に示されているように、電場印加なしのときの各々の G 曲線の共通接線において得られる組成 次に、Fig.2c に示されている晶出相の分布から、3 MHz の交流電場下では、 電場印加なしと比べるとスフェルライトの形成が起こり易いように見て取れる。 この結果を基に、Fig.3d に示されているように、3 MHz 印加時では、 スフェルライトの G 曲線の変化はバルク結晶のものよりも大きかったと考えられる。 したがって、3 MHz では、スフェルライトの誘電率、 一方、1 MHz 印加時では、得られた晶出相の分布(Fig.2b)は、電場印加なしと比べてバルク結晶の形成が起こり易いことが見て取れる。 このことは、Fig.3c に示されているように、交流電場を印加することによって、 バルク結晶の G 曲線の変化がスフェルライトのものよりも大きかったことを示唆している。 ゆえに、1 MHz では、バルク結晶の誘電率、 このように、本育成技術は、タンパク質結晶間の誘電分散の違い(Fig.1b)を利用することによって、 交流電場を用いて固相間の誘電率の大小関係を操作し、固相間の化学ポテンシャルに付加される静電エネルギーの大きさを変えることにより、 タンパク質結晶の多形制御を可能とする。 |
|
|
Fig.3 Molar free energy diagrams of the liquid phase and two solid α and β phases.
(a) Solid-liquid equilibrium, (b) driving force for nucleation without an electric field,
(c) driving force for nucleation with application of an electric field
[ |